Energia
Scenari energetici: il Sodio si prepara a sfidare il litio nel futuro delle batterie a stato solido

Per anni, il litio è stato il re incontrastato dell’accumulo energetico, alimentando i nostri smartphone, i laptop e, sempre più spesso, le nostre auto elettriche. Ma, si sa, i re non sono eterni, e l’oro bianco ha i suoi talloni d’Achille: è raro, costoso e la sua estrazione non è esattamente una passeggiata ecologica. Ora, però, un’alternativa più populista e abbondante bussa alla porta: il Sodio.
Un recente studio pubblicato sulla rivista Joule e condotto da ricercatori dell’Università della California, San Diego (UCSD), in collaborazione con la University of Chicago, ha messo a punto un’innovazione che potrebbe riscrivere le regole del gioco: batterie a stato solido basate sul sodio che mantengono le loro performance anche a temperature sotto zero. Un dettaglio non da poco, se pensiamo ai climi più rigidi dove l’efficienza delle batterie tende a scendere vertiginosamente.
Il problema del sodio (e come lo hanno risolto)
Il sodio è un’alternativa quasi ideale: è economico, abbondante (basta pensare al sale marino!) e la sua estrazione è meno impattante. Il problema, finora, è che le batterie a stato solido al sodio non sono riuscite a eguagliare le prestazioni di quelle al litio, soprattutto a temperatura ambiente. Un bel limite per una tecnologia che aspira a motorizzare le nostre vite.
Il breakthrough dei ricercatori, tra cui la professoressa Y. Shirley Meng e il professore Shyue Ping Ong, è stato aggirare il problema della scarsa conduttività ionica a temperatura ambiente con una mossa da manuale della chimica-fisica: la stabilizzazione cinetica di una struttura instabile, o metastabile.
Come hanno fatto?
- Hanno preso una forma metastabile di idridoborato di sodio ().
- L’hanno riscaldata fino al punto in cui stava per cristallizzare.
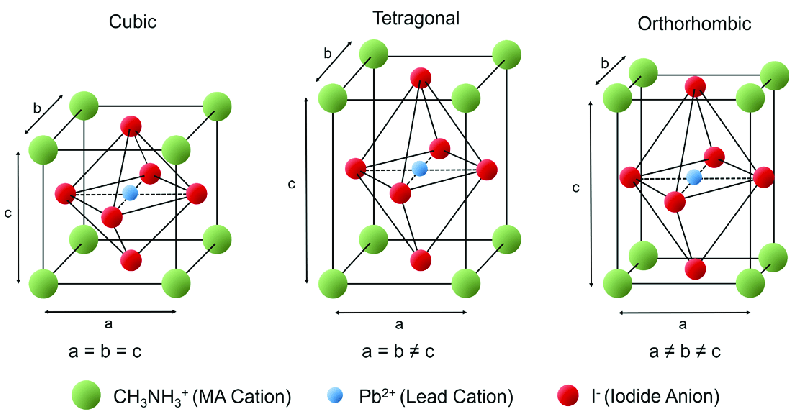
- L’hanno raffreddata rapidamente, bloccando cineticamente la struttura cristallina in una fase ortorombica ad alta mobilità ionica ().
Una struttura ortorombica è una struttura in cui gli angoli delle basi sono tutti perfettamente perpendicoalri, per cui la struttura ha, come base, dei rettangoli che risultano perfettamente ortogonali.
Questa fase metastabile, come spiegato dal co-primo autore Sam Oh, ha una conduttività ionica molto più elevata rispetto a quanto riportato in letteratura, rendendo il sodio un concorrente serio per le prestazioni elettrochimiche.
Un’innovazione tutta “Carne” e poca “Ossa”
L’ingegneria non si è fermata al solo elettrolita solido. La vera astuzia è stata l’abbinamento di questa fase metastabile con un catodo O3-type rivestito con un elettrolita solido a base di cloruro. Questa combinazione ha permesso di realizzare catodi spessi ad alto carico areale, un elemento cruciale per aumentare la densità energetica teorica della batteria.
- Catodo Sottile: Molto materiale inattivo e poca “carne” (materiale attivo).
- Catodo Spesso (Nuova Design): Meno materiali inattivi e molta più “carne” di catodo, migliorando l’energia immagazzinata per unità di area.
Questo approccio non solo migliora l’efficienza, ma è anche trasferibile ad altre chimiche simili, fornendo una strategia di progettazione pratica.
Non è una guerra: litio e sodio
Nonostante l’entusiasmo per il sodio, i ricercatori non vedono questo come un “sodio contro litio”. Come sottolinea la Professoressa Meng: “Abbiamo bisogno di entrambi“. L’obiettivo è che le future gigafactory siano in grado di produrre soluzioni di accumulo basate su entrambe le chimiche, utilizzando ogni materiale dove è più efficiente ed economico. Ogni soluzione avrà un suo diverso uso a seconda della situazione.
Questo lavoro, che ha sfruttato anche l’AI e il machine learning per la scienza dei materiali, non è solo un passo avanti per la chimica di base, ma è un’apertura concreta verso una diversificazione delle fonti di accumulo, fondamentale per un’economia energetica moderna e meno dipendente da risorse limitate. Il sodio, insomma, sta uscendo dall’ombra, pronto a dare il suo contributo all’elettrificazione del pianeta.
Domande e Risposte (Q&A)
1. Perché è così importante che le batterie funzionino bene a temperature sotto zero?
Le temperature molto basse tendono a rallentare la mobilità degli ioni all’interno dell’elettrolita, riducendo drasticamente la capacità e l’efficienza di una batteria (il classico problema in inverno). Per l’alimentazione dei veicoli elettrici (EV) e per lo stoccaggio di energia di rete in climi freddi, una batteria che mantiene le prestazioni sotto zero è essenziale. Questa innovazione rende il sodio un’alternativa più affidabile e versatile, estendendone il potenziale di utilizzo globale, anche in paesi nordici o regioni montane.
2. Cos’è la “stabilizzazione cinetica” e perché è la chiave di volta?
La stabilizzazione cinetica è una tecnica che impedisce a un materiale di raggiungere la sua forma più stabile, ma meno funzionale, a favore di una forma metastabile (temporaneamente stabile) con prestazioni superiori. In questo caso, la forma metastabile dell’idridoborato di sodio ha una struttura cristallina che permette agli ioni sodio () di muoversi molto più velocemente. Il “trucco” è stato un raffreddamento molto rapido (tempra) che ha bloccato la struttura in questa fase più performante, superando il limite di scarsa conduttività delle precedenti batterie al sodio.
3. In che modo questa ricerca combatte l’impatto ambientale e la scarsità del litio?
L’estrazione del litio è energivora e spesso causa danni ambientali significativi (consumo idrico, contaminazione del suolo). Sostituire o affiancare il litio con il sodio offre un duplice vantaggio: il sodio è abbondante in natura (nel sale marino, ad esempio) e la sua estrazione è meno distruttiva. Questa ricerca, rendendo il sodio competitivo, apre la porta a una diversificazione che riduce la pressione sulla limitata offerta di litio e mitiga l’impatto ambientale dell’industria delle batterie, allineandosi a un modello economico più sostenibile.







You must be logged in to post a comment Login