Economia
Addio impianti dentali? La scienza studia come far ricrescere i denti
La fine degli impianti in titanio potrebbe essere vicina. Una ricerca giapponese ha avviato la prima sperimentazione sull’uomo di un farmaco capace di stimolare la ricrescita naturale dei denti. Scopri come funziona questa rivoluzione odontoiatrica e quando potrebbe diventare realtà.

La perdita di un dente in età adulta è un’esperienza comune, dovuta a carie, malattie o traumi. Per milioni di persone, la soluzione è la stessa da secoli: una protesi artificiale. Sebbene la tecnologia sia avanzata rispetto agli antichi denti in osso di bue degli Etruschi, gli impianti moderni in titanio non sono privi di problemi. Ma cosa succederebbe se, invece di sostituire un dente perso, potessimo semplicemente farlo ricrescere?
Questa domanda, posta circa vent’anni fa a Paul Sharpe, biologo craniofacciale del King’s College di Londra, ha cambiato la direzione della sua ricerca. Oggi, l’idea di far ricrescere denti vivi e funzionali non è più solo fantascienza. Diversi gruppi di ricerca hanno ottenuto risultati promettenti in laboratorio e in Giappone è persino in corso una sperimentazione clinica su un farmaco che promette di rigenerare i denti direttamente nella bocca del paziente. Potremmo essere di fronte a una rivoluzione odontoiatrica, ma la strada non è priva di ostacoli.
I limiti degli impianti moderni
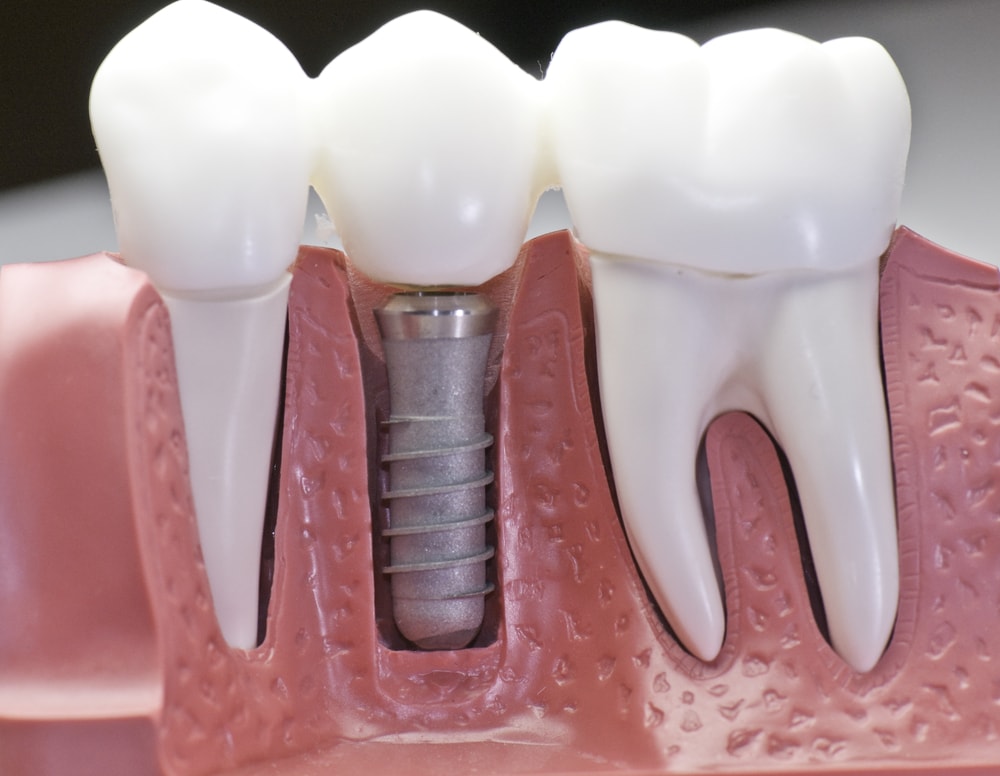
Oggi, il trattamento più comune per un dente perso è l’impianto in titanio. Questa pratica si basa su una scoperta casuale degli anni ’50, quando si notò che il titanio poteva fondersi con il tessuto osseo, un processo noto come osteointegrazione. Sebbene efficaci, questi impianti presentano notevoli svantaggi.
Essendo di metallo, non trasmettono alcuna sensazione durante la masticazione. A differenza dei denti naturali, che sono collegati all’osso mascellare tramite legamenti che assorbono parte della forza, gli impianti la trasmettono direttamente all’osso.
Come spiega Pamela Yelick, ortodontista della Tufts University, “non c’è nulla che ammortizzi le forze della masticazione”. Questo stress costante può portare al deterioramento dell’osso circostante, causando infiammazione, dolore e, nel tempo, il fallimento dell’impianto stesso. Un dente biologico, vivo e integrato, sarebbe invece più duraturo, funzionale e meno soggetto a infezioni.
Le nuove frontiere della rigenerazione dentale
Per creare un dente sostitutivo, è necessario replicare il complesso processo naturale che richiede l’interazione di due tipi di cellule: quelle epiteliali, che formano lo smalto, e quelle mesenchimali, che danno origine a dentina e polpa. La sfida principale è che le cellule epiteliali dentali scompaiono quasi del tutto dopo l’eruzione dei denti permanenti. La ricerca sta seguendo principalmente tre strade per superare questo problema.
- Ingegneria tissutale: Il team di Pamela Yelick utilizza delle “impalcature” biologiche, simili a gemme dentali private delle loro cellule originarie, che vengono poi “seminate” con una miscela di cellule dentali umane e animali. Impiantate in modelli animali, queste strutture si sono sviluppate in “tessuti simili a denti”, dimostrando la fattibilità del concetto.
- Riprogrammazione cellulare: Paul Sharpe e il suo gruppo stanno adottando un approccio diverso. Invece di usare impalcature, cercano di “convincere” le cellule adulte a comportarsi come quelle embrionali, riattivando i processi di sviluppo dentale. L’obiettivo è mappare e replicare la complessa serie di segnali chimici che le cellule si scambiano durante la formazione del dente, inducendo le popolazioni cellulari adulte a iniziare il processo.
- Un farmaco per “accendere” la crescita: La via forse più promettente arriva dal Giappone. Un gruppo di ricercatori guidato da Katsu Takahashi ha identificato un gene, chiamato USAG-1, che agisce come un interruttore, inibendo lo sviluppo dei denti. Bloccando l’azione della proteina prodotta da questo gene, sono riusciti a far crescere nuovi denti nei topi.
Sulla base di questa scoperta, la società biofarmaceutica Toregem Biopharma ha sviluppato un farmaco a base di anticorpi e, nel 2024, ha avviato la prima sperimentazione clinica di fase I su uomini adulti sani a cui manca almeno un dente. L’obiettivo è testarne la sicurezza e il dosaggio.
Tra ostacoli economici e speranze concrete
Se la tecnologia esiste, perché non è ancora disponibile? La risposta risiede in due fattori principali: la complessità biologica e, soprattutto, i costi. La ricerca odontoiatrica è storicamente sottofinanziata rispetto ad altri settori medici come l’oncologia o la cardiologia. Sviluppare queste terapie richiede investimenti enormi per la ricerca e le sperimentazioni cliniche, e il costo finale per il paziente dovrebbe essere competitivo con quello di un impianto tradizionale. Senza considerare che queste nuove tecnologie manderebbero in soffitta quelle implatologiche, su cui sono stati investiti miliardi.
Nonostante le sfide, l’ottimismo prevale. La sperimentazione di Toregem Biopharma rappresenta un passo avanti cruciale, con l’azienda che spera di portare il farmaco sul mercato entro il 2030, inizialmente per trattare bambini con edentulia congenita, una condizione genetica che impedisce la crescita dei denti.
La domanda non è più “se” saremo in grado di far ricrescere i denti, ma “quando”. Molti ricercatori ritengono che, entro il prossimo decennio, potremmo assistere all’arrivo delle prime terapie biologiche in grado di offrire un’alternativa viva e permanente agli impianti metallici.






You must be logged in to post a comment Login